| Tabs Page |
|---|
| id | Description |
|---|
| title | Description |
|---|
| Microscope droit Olympus BX63Pavillon P-G Desmarais, Local 5308-2
Tarif d'utilisation Microscope simpleAvancé tier 1 Instrument octroyé au Dre Marina Martinez par la Fondation Canadienne pour l'Innovation (FCI). - Applications
- Lumière transmise
- Contraste de phase
- Lumière polarisée. DIC
- Fluorescence
- Caméra couleur
Sources lumineuses
| Développer |
|---|
| title | Caractéristiques complètes de la X-Cite NOVEM XT910 complete specifications |
|---|
|
| Source | Excitation wavelengths |
|---|
Pic d'émission Puissance | Compatible fluorophores | Nominal power (mW) |
|---|
395404303515 | | 510 | 20 | | 550 | 20 | | 580 | 20 | | 640 | 20 | | 730 | 10 |
Spécifications Lumencor SOLA (anglais).pdf
|
| FITC, GFP |
| | 500-600 | -
[500-600] |
|
| 509/22
[498-520] | YFP |
| 554/23
[542-565] | TRITC |
| 578/21
[567-588] | mCherry |
| | 635 |
| Cy5
|
| 735 |
| Cy7 |
|
|
Objectifs 4x/0.16 Air WD TBD16 10x/0.4 Air WD TBD3.1 - 20x/0.75 Air WD TBD0.6
40x/0.95 Air WD TBD0.18 60x/1.35 Huile WD TBD0.15 - 100x/1.4 Huile WD TBD00.213
- Vide
| Développer |
|---|
| title | Caractéristiques complètes des objectifsObjectives complete specifications |
|---|
|
| Position | Nom | Marque | Nom complet | Identifiant | Ouverture numérique | Immersion | Distance de travail (mm) | Transmittance
(% [nm]) | Technique | Épaisseur du couvre-objet (mm) |
|---|
| 1 | 4x/0.16 Air | Olympus | 4x/0.16 Air UPlanSApo | | 0.16 | Air |
TBD | TBD | TBD| 16 | >90% at 550nm
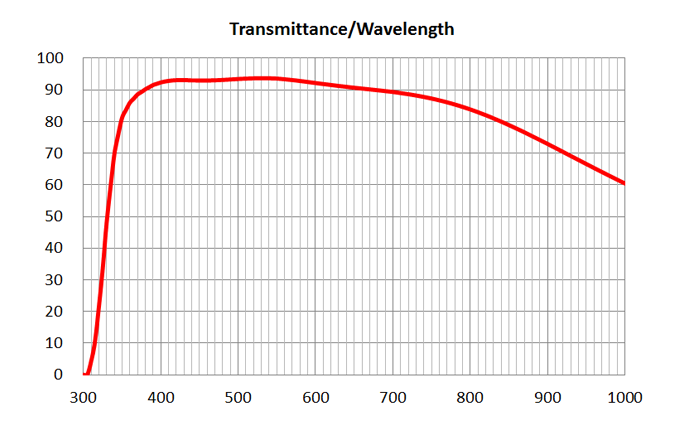 Image Added Image Added | BF, Fluo | - | | 2 | 10x/0.4 Air | Olympus | 10x/0.4 Air
UPlanSApo | UPLXAPO10X.pdf | 0.4 | Air |
| 3.1 | ~90% at 550nm
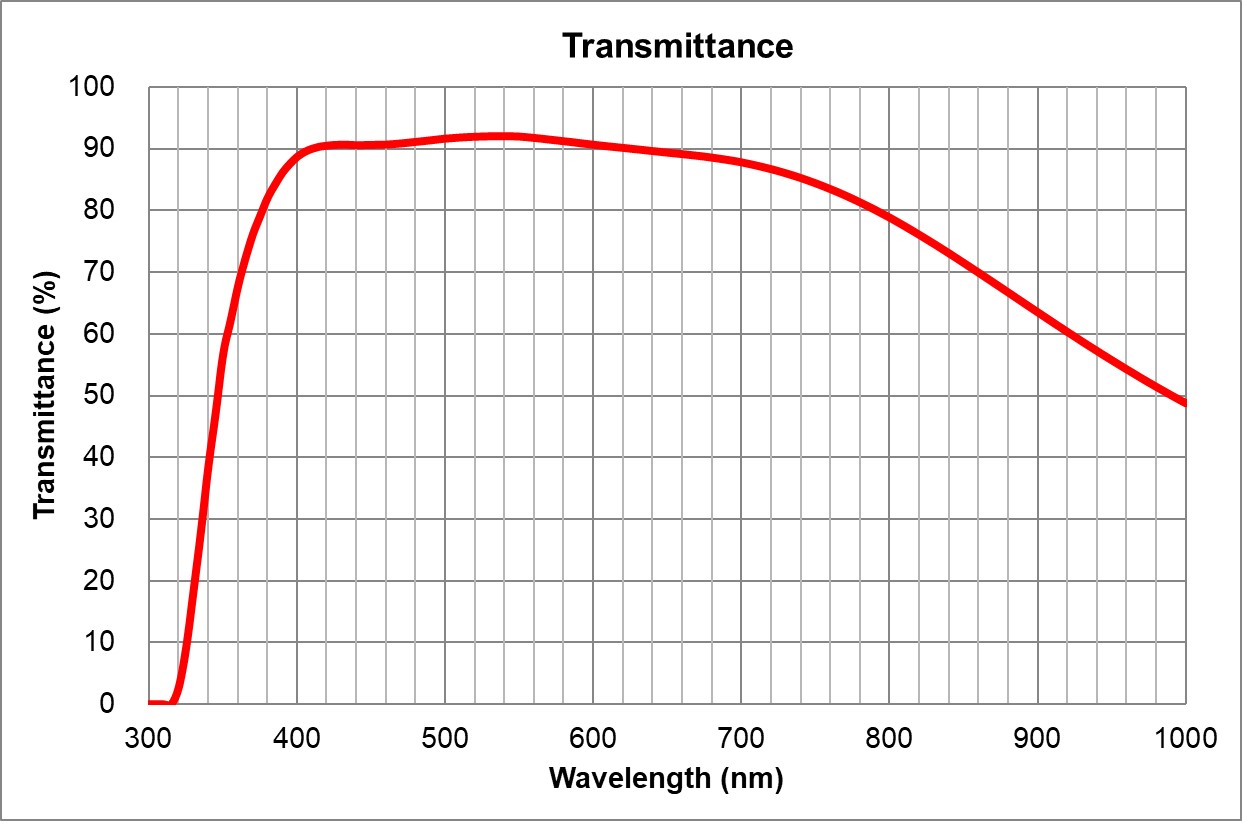 Image Added Image Added | BF, Pol, DIC, Fluo |
TBD | TBD | TBD | 0.17 | | 3 | | Olympus | 20x/0.75 Air
UPlanSApo | | 0.75 | |
TBD | TBD | | 0.6 | >90% at 550nm
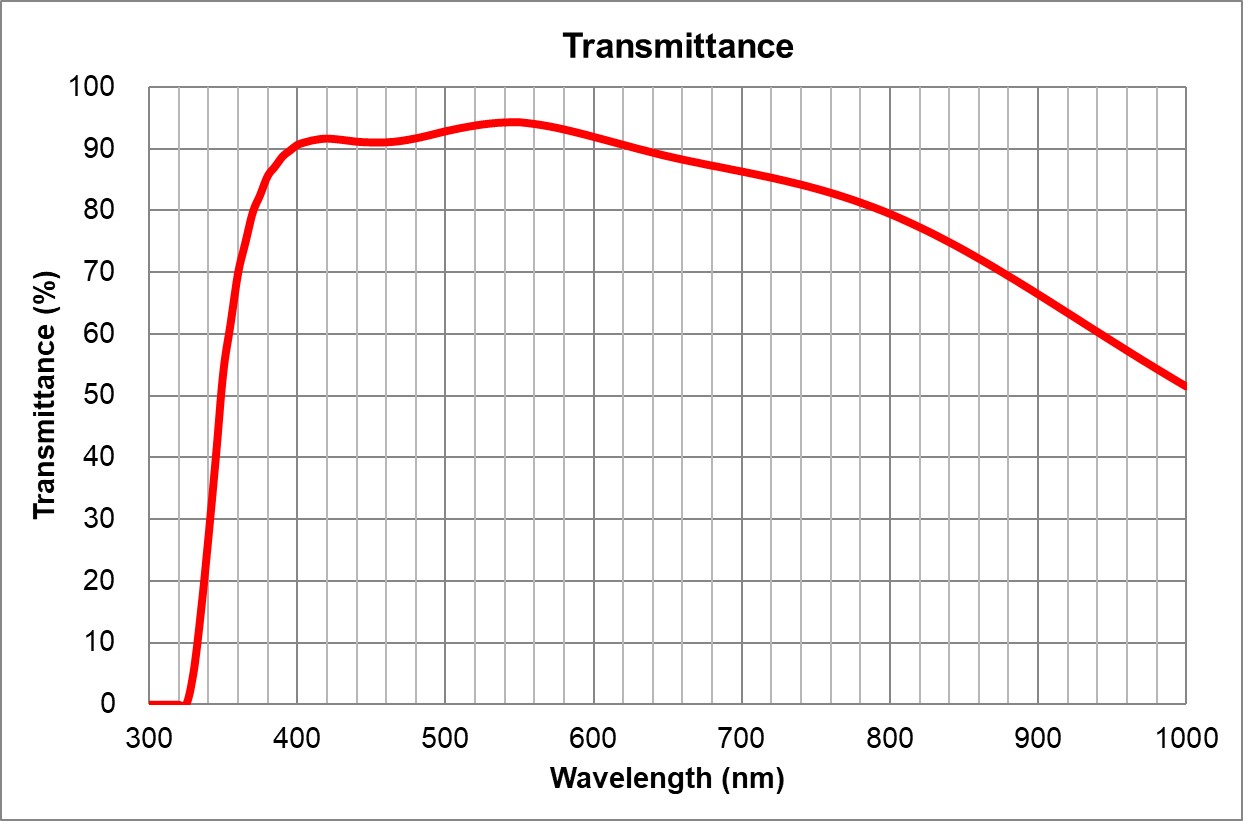 Image Added Image Added | BF, Pol, DIC, Fluo |
TBD | 0.17 | | 4 | 40x/0.95 Air | Olympus | 40x/0.95 Air
UPlanSApo | | 0.95 | Air |
TBD | TBD | TBD | Ajustable | 0.18 | ~90% at 550nm
 Image Added Image Added | BF, Pol, DIC, Fluo | Adjustable 0.11-0.23 | | 5 | 60x/1.35 Huile | Olympus | 60x/1.35 |
Oil | Huile | TBD | TBD | TBD | 0.15 | ~90% at 550nm
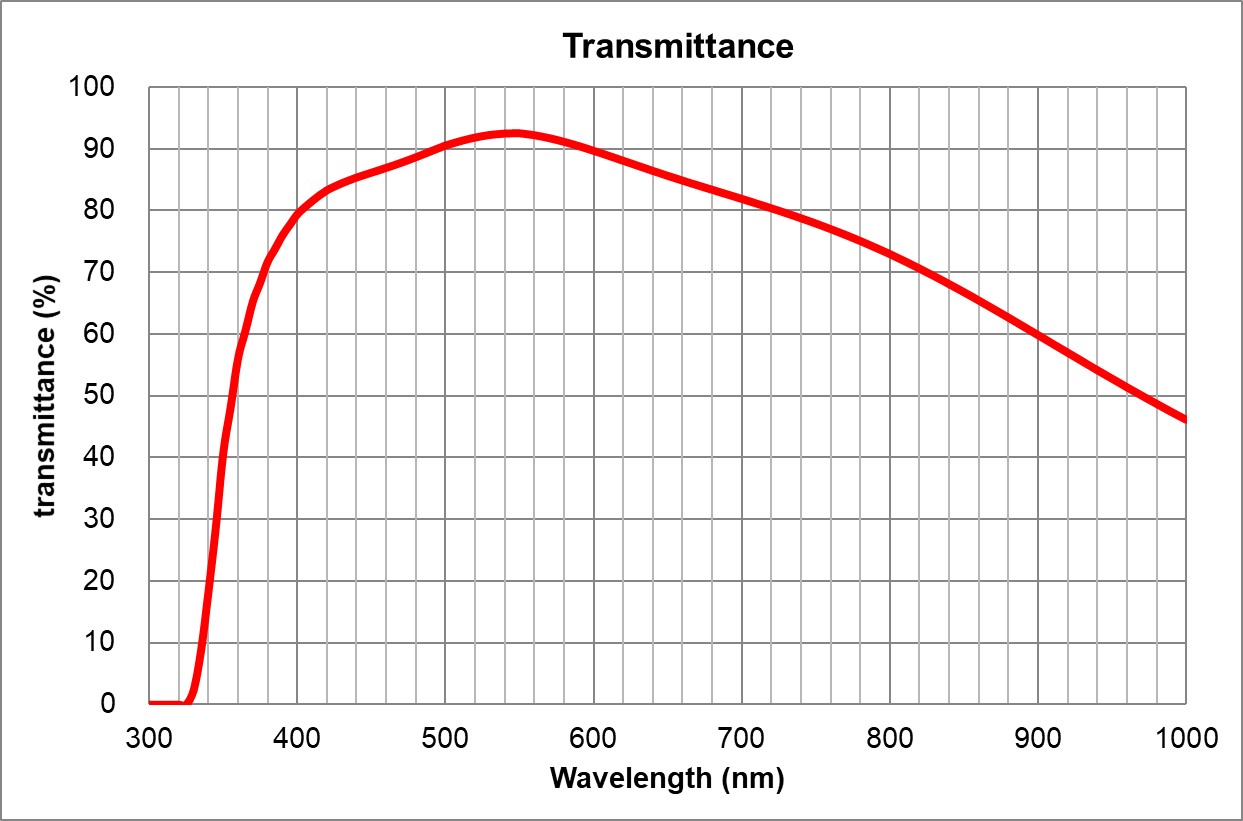 Image Added Image Added | BF, Pol, DIC, Fluo | 0.17 | | 6 | | Olympus | 100x/1.4 |
Oil | Huile | TBD | TBD | TBD | 0.13 | ~90% at 550nm
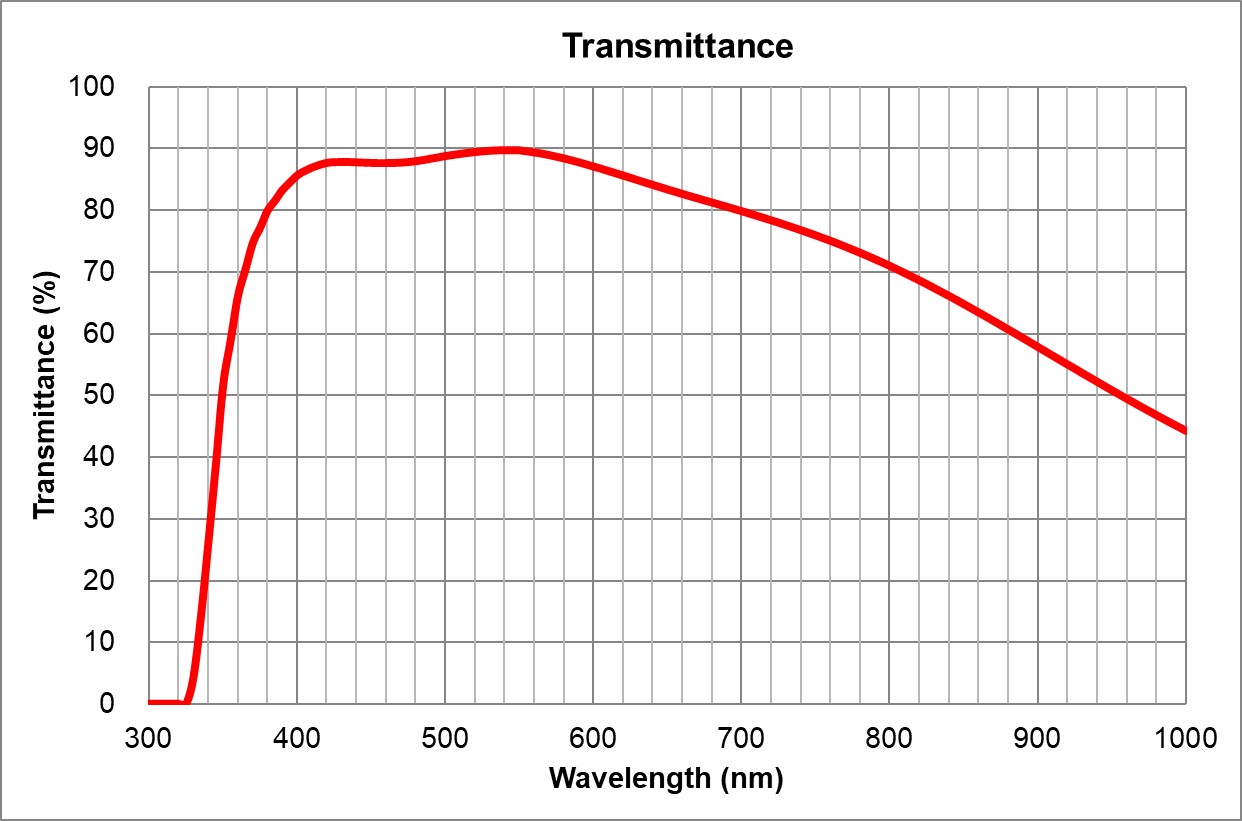 Image Added Image Added | BF, Pol, DIC, Fluo | 0.17 | | 7 | |
|
|
|
| |
|
|
|
|
BF: Champ clair ( Bright-field)
Pol: Lumière polarisée
PhC: Contraste de phasePolarized light
DIC: Differential interference contrast
Fluo: Fluorescence |
- Cubes de filtres
- Vide
- DAPI
- FITC
- TRITC
- TxRed
- mCherry
- DAPI/FITC/TRITC/Cy5/Cy7Vide
- Vide
- u-FDI CT
| Développer |
|---|
| title | Caractéristiques complètes des filtresFilters complete specifications |
|---|
|
NomMarque| Identifiant | Filtre d'excitation | Miroir dichroïque | Filtre d'émission | Commentaire | 1 | DAPI/Hoechst/AMCA | Chroma | Cube set 31000v2 | 350/50x
[325-375] | 400LP | 460/50m
[435-485] | 2 | FITC/EGFP | Chroma | Cube set 41001 | 480/40x
[460-500] | 505LP | 535/50m
[510-560] | 3 | TRITC/Rhodamine | Chroma | Cube set 41002c | 545/30x
[530-560] | 570LP | 620/60m
[590-650] | 4 | Texas Red | Chroma | Cube set 41004 | 560/55x
[532-588] | 595LP | 645/75m
[607-682] | 5 | Vide | 6 | Vide | | ID | Excitation Filter | Dichroic mirror | Emission Filter | Comments |
|---|
| 1 | Empty |
|
|
|
|
|
| | 2 | DAPI | Olympus | U-FUNA | 360-370 | 410LP | 420-460 |  Image Added Image Added
| | 3 | FITC | Olympus | U-FBNA | 470-495 | 505LP | 510-550 |  Image Added Image Added
| | 4 | TRITC | Olympus | U-FGWA | 530-550 | 570LP | 575-625 |  Image Added Image Added
| | 5 | mCherry | Olympus | U-FYW | 540-585 | 595LP | 600LP |  Image Added Image Added
| | 6 | DAPI/FITC/TRITC/Cy5/Cy7 |
| LED DA/ FI/TR/CY5/C Y7-5X-A-000 | 5 filters within the Novem FF01-387/11 FF02-485/20 FF01-560/25 FF01-650/13 FF01-740/13
| FF408/504/581/667/762-Di01 | FF01-440/521/607/694/809 |
| | 7 | Empty |
|
|
|
|
|
| | 8 | DIC Analyzer | Olympus | U-FDICT DIC | - | - | - | DIC Analyzer |
|
- Détecteur
- Olympus DP80 double détecteur (couleur et monochrome) camera CCD, 6.45 x 6.45 um pixel size,15 images/s à résolution maximale, 55% QE at 550nm
Mode couleur 4080 x 3072 pixels, 24-bit
Mode Monochrome 1360 x 1024 pixels, 14-bit
Olympus_DP80 Camera_User Guide-1.pdf
Détecteur- Caméra couleur Olympus DP80 x pixels, 14-bit,
|
| Tabs Page |
|---|
| id | Guide d'utilisation |
|---|
| title | Guide d'utilisation |
|---|
|
| UI Expand |
|---|
| expanded | true |
|---|
| title | Démarrage |
|---|
| - Retirez la housse de protection du microscope
- Allumez l’ordinateur (#1)
- Allumez la multiprise d’alimentation du microscope (#2)
Allumez l'ecran tactile du microscope (l’interrupteur est à sur le côté droit du microscope (#3) Utilisez vos identifiants UdM pour vous connecter à Windows
Démarrez le logiciel CellSens Dimension
| Info |
|---|
Lors de la première utilisation il est nécessaire d’importer les paramètres du microscope dans le logiciel. Pour ce faire, suivre les instructions |
| | UI Expand |
|---|
| - Enregistrez vos données
- Fermez le logiciel NIS-Elements
- Transférez vos données sur le disque D: (Data Storage) ou sur votre disque dur externe et les supprimer du disque local C:
- Éteindre l'ordinateur
- Si utilisé, nettoyez l’objectif à huile avec du nettoyant et du papier à lentille
- Éteindre la multiprise d’alimentation du microscope (#2)
- Couvrir l’instrument avec la housse de protection
| Remarque |
|---|
| - Récupérez vos échantillons notamment ceux dans le microscope
- Laissez le microscope et l’espace de travail propre
|
Démarrez le logiciel CellSens Dimension
|
| UI Expand |
|---|
| - Les fichiers peuvent être sauvés temporairement (pendant l’acquisition) sur le disque local C: (bureau)
- À la fin de chaque session, copiez vos données sur votre disque externe et supprimez-les du disque local C:
- Vous pouvez stocker vos fichiers sur le disque D: (Data Storage). Si vous utilisez ce disque, veuillez créer un dossier par laboratoire en utilisant le nom de famille du chercheur principal. À l’intérieur, créez un dossier par utilisateur (Prénom_Nom).
| Remarque |
|---|
Dans tous les cas, ne stockez pas vos fichiers sur le disque C: |
| UI Expand |
|---|
| title | Paramétrage du logiciel |
|---|
| | Lors de la première utilisation, il est nécessaire d’importer dans le logiciel les paramètres spécifiques au microscope. Cette procédure est habituellement réalisée lors de la séance de formation.
Il est cependant également possible de l’utiliser pour réinitialiser le logiciel si celui-ci ne s‘affiche pas correctement par exemple. | Remarque |
|---|
Attention, cette procédure supprimera tous vos protocoles d’expérience et rétablira les paramètres originaux du logiciel. |
- Si ouvert, fermez le logiciel NIS-Elements et attendre logiciel CellSens Dimension et attendre sa fermeture complète (jusqu’à 30 secondes)
- Sur le le Bureau ouvrez ouvrez le dossier Softwares
- Ouvrez le logiciel NIS Settings Utility
- Cliquez sur l’onglet Import
- Cliquez sur Browse
- Naviguez jusqu’à votre bureau
- Sélectionnez le fichier Nikon-E600 Settings.bin
- Cliquez Open
- Sélectionnez tous les items
- Cliquez Import
- Cliquez OK
- dossier Documentation
- Double-cliquez sur Settings for BX-63
- Un script s'excutera et une fenêtre noire apparaitra brièvementFermez le logiciel NIS Settings Utility
- Vous pouvez ensuite réouvrir le logiciel NIS-Elementslogiciel CellSens Dimension
|
| UI Expand |
|---|
| title | Procédure pour le chargement des échantillons |
|---|
| Cette procédure vous permettra permet de mettre le microscope dans une configuration sécuritaire pour pouvoir charger votre échantillon et d'effectuer une calibration de la mise au point. À la fin de cette procédure , le microscope sera prêt pour l'acquisition.
| UI Expand |
|---|
| title | Première mise au point |
|---|
| Sur |
le Sélectionnez l'objectif 4xl’écran tactile du microscope : |
Tournez la molette principale d'ajustement de la mise au point pour faire descendre la platine dans sa position la plus bassePlacez votre échantillon sur la platine du microscope avec le couvre-objet vers l'objectif- Appuyez sur Full Operation
Appuyez sur 4x pour sélectionner l'objectif 4x
|
| Info |
|---|
L’objectif 4x est le plus sécuritaire car il possède la plus grande distance de travail ( |
|
17 16 mm). L'échantillon apparaitra parfaitement net bien avant que l'objectif ne s'approche de celui-ci. Il est recommandé |
|
de de toujours faire la première mise au point avec l'objectif le plus sécuritaire. Les objectifs sont para-focaux, faire la mise au point avec l'objectif le plus sécuritaire vous permettra ensuite de trouver facilement votre échantillon avec un autre objectif. |
|
Sélectionnez le mode d'imagerie désiré (Champs clair ou Fluorescence). Vous trouverez dans l'onglet Trajet lumineux de cette page, les schémas qui vous permettront de suivre la lumière tout le long de son chemin au travers les différentes composantes du microscope. Ces schémas vous aideront à configurer le microscope pour le mode d'imagerie désiré.
| Info |
|---|
Assurez-vous que la lumière soit bien visible aux oculaires avant de continuer. |
- Appuyez sur Escape pour faire monter les objectifs dans leur position la plus haute
Placez la lame de test sur la platine du microscope avec le couvre-objet vers l'objectif
| Remarque |
|---|
| Toujours utiliser la lame de test pour effectuer la première mise au point. |
- Si nécessaire, déplacez la platine pour que l'échantillon soit centré sur l'objectif
Sur l’ordinateur : Ouvrez le logiciel CellSens Dimension - Attendre l'ouverture du logiciel (oui c'est long...)
En bas à droite de la fenêtre, sélectionnez BF ou la fluorescence désirée (DAPI, FITC, TRITC ou mCherry) pour activer la configuration Ajustez
|
Ajustez la mise au point avec la molette principale tout en regardant dans les oculaires jusqu'à ce que l'image soit parfaitement nette | Remarque |
|---|
La mise au point est aux alentours de Z = 19000 um. La valeur de la position en Z est visible sur l'écran tactile. |
- En bas à droite de la fenêtre, sélectionnez Off pour éteindre l'illumination
|
| UI Expand |
|---|
| title | Mise au point secondaire |
|---|
|
| note | Faire d’abord la première mise au point avec l'objectif le plus sécuritaire avant de sélectionner un autre |
objectif et objectif et de poursuivre avec la mise au point secondaire. |
| UI Expand |
|---|
| title | Mise au point avec les objectifs à air |
|---|
| Après avoir effectué la première mise au point, sur |
le l’écran tactile du microscope : |
Sélectionnez Appuyez sur 10x, 20x ou 40x pour sélectionner l'objectif
|
à air (4x, 10x, 20x, 40x ou 60x) 60x est le 40x est le meilleur objectif à Air car il possède le plus grand nombre de corrections optiques (Plan Apochromat) et la plus grande ouverture numérique (0. |
|
8595). Il offre une résolution latérale de |
|
448nm 420nm à une longueur d'onde de 550nm. |
- En bas à droite de la fenêtre, sélectionnez BF ou la fluorescence désirée (DAPI, FITC, TRITC ou mCherry) pour activer la configuration
Ajustez la mise au point avec la molette de précision tout en regardant dans les oculaires jusqu'à ce que l'image soit parfaitement nette - Sélectionnez Off pour éteindre l'illumination
- Votre échantillon est prêt pour
|
l’acquisition
| UI Expand |
|---|
| title | Mise au point avec les objectifs à l'huile |
|---|
| Après avoir effectué la première mise au point, sur |
le | Info |
|---|
L’objectif l’écran tactile du microscope : |
Tournez la tourelle des objectifs pour vous placer entre les objectifs 60x et 100x (cela vous laissera de la place pour l'étape suivante)
Appuyez sur 60x Oil (1.35), 100x Oil (1.4) pour sélectionner l'objectif désiré. Le microscope relèvera automatiquement les objectifs pour que l'échantillon soit accessible.
|
100x est le meilleur objectif à l'huile car il possède le plus grand nombre de corrections optiques (Plan Apochromat) et la plus grande ouverture numérique (1.4). Il offre une résolution latérale de 240nm à une longueur d'onde de 550nm. |
- Déposer une goutte d’huile sur votre échantillon
|
Tournez la tourelle des objectifs pour placer l'objectif 100x au dessus de l'échantillon
Dans le logiciel CellSens Dimension : - Cliquez sur OK
- En bas à droite de la fenêtre, sélectionnez BF ou la fluorescence désirée (DAPI, FITC, TRITC ou mCherry) pour activer la configuration
- Ajustez la mise au point avec la molette de précision tout en regardant dans les oculaires jusqu'à
|
ce que - ce que l'image soit parfaitement nette
- Sélectionnez Off pour éteindre l'illumination
- Votre échantillon est prêt pour l’acquisition !
|
|
|
| UI Expand |
|---|
| - Les fichiers peuvent être sauvés temporairement (pendant l’acquisition) sur le disque local C: (bureau)
- À la fin de chaque session, copiez vos données sur votre disque externe et supprimez-les du disque local C:
- Vous pouvez stocker vos fichiers sur le disque D: (Data Storage). Si vous utilisez ce disque, veuillez créer un dossier par laboratoire en utilisant le nom de famille du chercheur principal. À l’intérieur, créez un dossier par utilisateur (Prénom_Nom).
| Remarque |
|---|
Dans tous les cas, ne stockez pas vos fichiers sur le disque C: |
|
| UI Expand |
|---|
| - Enregistrez vos données
- Fermez le logiciel CellSens Dimension
- Transférez vos données sur le disque D: (Data Storage) ou sur votre disque dur externe et les supprimer du disque local C:
- Éteindre l'ordinateur
- Si utilisé, nettoyez les objectifs à huile avec du nettoyant et du papier à lentille
- Éteindre la multiprise d’alimentation du microscope (#2)
- Couvrir l’instrument avec la housse de protection
| Remarque |
|---|
| - Récupérez vos échantillons notamment ceux dans le microscope
- Laissez le microscope et l’espace de travail propre
|
|
|
| Tabs Page |
|---|
| id | Trajet lumineux |
|---|
| title | Trajet lumineux |
|---|
|
Les schémas suivants permettent de suivre le trajet lumineux en lumière transmise (fond clair, contraste de phase et lumière polarisée) et en lumière réfléchie (fluorescence).viewpdf
LightPath_Nikon E600| Olympus_BX63_Lightpath.pdf | | height | 250 |
|---|
|
|
| Tabs Page |
|---|
|
Manuels disponibles version anglaise.
|
| Tabs Page |
|---|
| id | Fiche Technique |
|---|
| title | Fiche Technique |
|---|
|
Section disponible dans la version anglaise.
|
| Tabs Page |
|---|
| id | Dépannage et FAQ |
|---|
| title | Dépannage et FAQ |
|---|
| Dépannage| UI Expand |
|---|
| title | Le logiciel NIS-Elements affiche un message d'erreur: Camera Driver...microscope ne s'allume pas, que dois-je faire? |
|---|
| Veuillez vous assurer que l’écran tactile du microscope est allumé. L'interrupteur n'est pas facilement accessible et se situe à l'arrière à droite de l'écran tactile. Ceci peut survenir lorsque le logiciel NIS-Elements ne parvient pas à établir la connexion avec la caméra par exemple lorsque la caméra n'est pas allumée. Fermez le logiciel NIS-ElementsAllumez la caméra (la multiprise du microscope et l'interrupteur sur le dessus de la caméra)Vérifiez la connexion USB entre la caméra et l'ordinateurAllumez le logiciel NIS-Elements |
FAQ| UI Expand |
|---|
| title | Puis-je utiliser ce microscope pour observer des cellules en culture? |
|---|
| Non. C'est un microscope droit conçu pour l'observation de spécimen montés entre lame et lamelles (d'épaisseur 0.17mm). |
Plus de dépannage et de FAQs sont disponibles dans la version anglaise. |
|









